地角天邊
江郎才盡,不足為訓http://www.xml-data.org/YSJSYKXGC/html/2017050014.htm
| 不同放電倍率磷酸鐵鋰電池循環性能研究 |
自鋰離子電池問世以來,有關它的研究和發展一直是全世界關注的焦點.鋰離子電池作為一種可重複使用的環保電池,它是通過鋰離子在正負極間相互脫嵌來完成電量轉化過程,具有循環壽命長、工作電壓高和能量密度大等許多優點[1-5].近年來,由於鋰離子電池技術的不斷進步,使得它在便攜式電子設備電動汽車和軍事航天等領域均獲得了廣泛的應用[6-8].在現有的各種電池體係中,磷酸鐵鋰電池的原料來源更加豐富、成本更低、循環壽命最長、安全性更好,無疑是目前最具發展潛力的電池體係[9-13].
電池的容量、能量、內阻和開路電壓等是反映其性能的重要指標,也是電池管理係統設計的重要參數.電池容量的變化規律,會直接影響到電池的壽命管理和荷電狀態估算[14-15];電池內阻大小的變化主要影響動力電池的功率和產熱特性[16-17];而開路電壓(Open circuit voltage, OCV)曲線可以參與電池荷電狀態的估算以及電池健康狀態的評價,便於電池的應用優化和性能維護, 進而提高電池管理係統(BMS)的使用效率[18-20].
文中研究了磷酸鐵鋰動力電池在不同放電倍率下的容量衰減情況,並且在循環過程中測試了對應條件下的電化學交流阻抗和電池開路電壓,分析了交流阻抗及開路電壓與電池循環圈數間的變化規律,為電池健康狀態的評價和電池壽命快速預測係統的建立提供技術上的支持.
1 實驗1.1 實驗電池及設備實驗采用的電池為天津力神公司生產的18650型商用LiFePO4鋰離子電池,標準電壓範圍2.0~3.65 V,標稱容量為1 350 mAh,標準放電倍率為0.2 C.用5 V/5 A藍電電池充放電測試係統(武漢產)進行充放電.恒溫箱為某國產高低溫調濕實驗箱,為電池充放電實驗提供恒定的環境溫度.交流阻抗測試采用瑞士萬通Auto Lab Pgstat302N電化學工作站.
1.2 實驗過程將待測電池放置於25 ℃恒溫幹燥箱中,使用不同放電倍率對電池進行放電實驗,充電過程采用先恒流再恒壓的模式,放電過程采用恒流模式,研究電池放電容量與放電倍率間關係.充電方式為,將電池以1 C電流恒流充電至電壓為3.65 V,轉恒壓充電至電流小於0.05 C(65 mA)時,停止充電.將電池充滿電後,在25 ℃的環境溫度下靜置1 h,再分別以0.1 C、0.2 C、0.5 C、1 C、1.5 C、2 C電流恒流放電至電壓為2.0 V時,停止放電,計算電池的放電容量.
適當的提高電池循環時環境溫度,可以加速電池的老化,減少測試時間,便於比較不同倍率下電池特性的變化規律.因此,在40 ℃環境溫度下對實驗電池進行不同倍率充放電循環實驗,充電方式均采用1 C恒流充電至上限電壓3.65 V,轉恒壓充電至電流小於0.05 C後,停止充電,靜置0.5 h.為了研究放電倍率對鋰離子電池的影響,將放電過程分為3組,靜置完成後,第1組以0.5 C恒流放電至下限電壓2.0 V後,停止放電,靜置0.5 h.以1次完整的充放電過程為1個周期,進行循環實驗.第2、第3組實驗分別采用1 C和2 C放電倍率進行循環實驗,其他條件均與第1組實驗相同.電池每循環50個周期時進行一次標準放電容量測定.當電池的循環周期達到0次、50次、100次、200次、300次、400次、500次時,進行一次交流阻抗測試.
標準放電容量測試的步驟如下:在25 ℃恒溫箱中,以1 C恒流充電至上限電壓3.65 V,轉恒壓充電至電流小於0.05 C後,停止充電,靜置0.5 h.再以1 C恒流放電至下限電壓2.0 V,停止放電,計算電池放出的容量.
交流阻抗測試(EIS),電池進行交流阻抗測試時均處於放空電狀態.實驗采用恒電勢EIS法,設置電勢值為電池開路電壓,掃描的頻率範圍為100 kHz~10 mHz,正弦電壓振幅值為10 mV,測試電池處於不同循環周期的交流阻抗譜,建立相應合適的等效電路進行擬合分析,得到電池各阻抗參數與循環周期間的變化規律.
2 結果與討論2.1 放電倍率對電池放電容量的影響圖 1所示為LiFePO4動力電池在25 ℃的環境溫度下分別以0.1 C、0.2 C、0.5 C、1 C、1.5 C和2 C不同倍率的放電曲線.可知,LiFePO4電池不同倍率下的放電過程均存在一個穩定的放電平台,平台電壓介於3.0~3.4 V之間,另外,平台電壓隨著放電倍率的增加而降低,這是因為放電倍率的增加,增大了電池的放電電流,又由於電池內阻的存在,造成電池放電時電壓將會增大.另一方麵,大倍率電流放電還會使電池的極化增大,也會使電池的電壓平台降低.
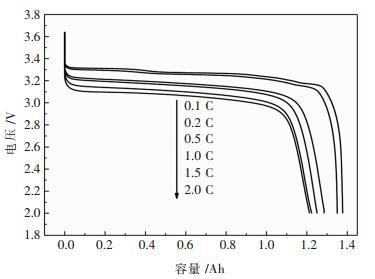 |
| 圖 1 LiFePO4電池不同倍率的放電曲線Fig. 1 Discharge curves of LiFePO4 batteryat different discharge at different discharge ratio |
LiFePO4電池在不同放電倍率下放電放出的容量如圖 2所示.電池放出的容量會隨著電池放電倍率的增加而減小.在0.1 C的小倍率下電池放出的容量比電池的標稱容量有所增大,而在2 C倍率下放電容量僅為標稱容量的90 %.由此說明,放電倍率與電池放出的容量之間具有一定的負相關性.
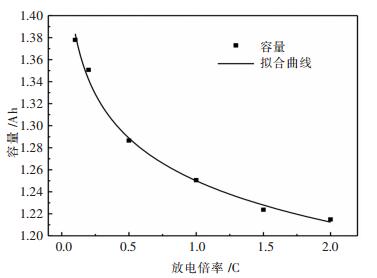 |
| 圖 2 放電容量隨放電倍率的變化曲線Fig. 2 Curve of discharge capacity with discharge rate |
1897年,Peukert [20]在對鉛酸電池的恒流放電試驗中發現恒流放電電流與持續放電時間/容量關係的經驗公式,其方程表示如下:
| Ip∗t=constant | (1) |
式(1) 中,I為放電電流,p為Peukert係數,t為最大放電時間.此公式給出了電池放電電流與最大放電時間的關係,但在實際應用過程中對於最大放電時間不好界定,研究人員對其進行修正,將電池最大放電時間與電池的放電容量聯係起來,推出了電池放出容量與電池電流滿足冪函數關係,而放電電流與放電倍率滿足線性對應關係,進一步得出電池放電容量與電池的放電倍率間滿足冪函數規律.
將電池放電容量與放電倍率進行曲線擬合,得到如下關係式:
| Q=1.250×K−0.044;X2=0.992 5 | (2) |
式(2) 中,Q是電池放電容量,K是放電倍率,X2是該擬合的相關係數.它表示擬合曲線與原數據的吻合程度,其數值在0~1之間,X2越大時,曲線擬合的吻合度就越好;反之,則擬合的越差. 圖 2中容量與放電倍率采用冪函數擬合後的擬合相關係數為0.992 5,說明容量與放電倍率之間是符合冪函數規律.
2.2 不同倍率循環的放電容量分析為了研究不同倍率循環過程中的放電容量變化規律,對不同循環次數的電池進行了充放電倍率均為1 C的容量測定. 圖 3所示為電池在40 ℃環境溫度下0.5 C、1 C和2 C倍率循環後每隔50次周期所測的標準放電容量.從圖 3中可知,電池在整個500次循環過程中放電容量呈現2個階段的變化趨勢.在循環前100圈,0.5 C、1 C和2 C倍率下的電池標準放電容量均逐漸上升,循環100次時放電容量達到最大值,在此階段電池的容量變化規律基本保持一致.但循環次數大於100次時,電池的放電容量才開始衰減,且不同倍率下的衰減程度不同.以循環100次測得電池最大放電容量為電池的額定放電容量,計算電池處於不同倍率循環周期時的容量衰減率,繪製容量衰減率與循環周期關係曲線,如圖 4所示. 500次循環周期後,2 C放電倍率的電池放電容量衰減率為其額定放電容量的12.8 %,放電倍率為0.5 C、1 C的電池放電容量衰減率分別達到6.3 %和9.6 %.在2 C倍率下循環的電池其容量衰減曲線斜率要高於0.5 C和1 C.由此表明,電池在較高倍率下循環容量衰減更快,放電倍率對電池的循環放電容量的影響很大.
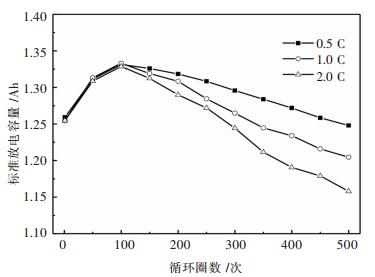 |
| 圖 3 電池放電容量與循環次數關係曲線Fig. 3 Relationship graph between discharge capacity with the number of cycles |
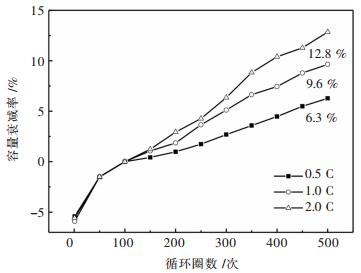 |
| 圖 4 不同倍率循環容量衰減曲線Fig. 4 Loss of capacity curve at different discharge rates cycle |
2.3 倍率循環中電池內阻變化
圖 5(a)、圖 5(b)和圖 5(c)分別為電池在40 ℃下,經過0.5 C、1 C和2 C放電倍率循環後,在放電態下不同循環周期的EIS圖譜,可知,所有EIS圖均是由高頻區的直線段、中高頻區的圓弧段和低頻區的斜線段3部分組成,分別對應感抗部分、電荷轉移部分和擴散部分的阻抗特征.前100次的電池循環過程中,3組放電倍率循環下的EIS圖整體均向左偏移,其中低頻區的擴散斜率偏移程度最大.在100~500次的循環過程中,組成EIS的各部分阻抗又逐漸增加.由此表明,電池在循環前期處於活化階段,活化結束後,繼續循環,電池處於逐漸衰退狀態.
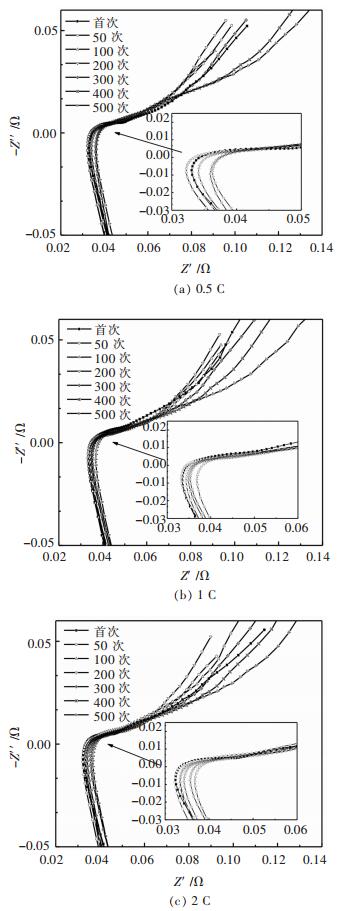 |
| 圖 5 不同倍率循環後放電態下的EISFig. 5 The EIS of discharge state after different discharge rates cycle |
為了研究循環過程中各部分的阻抗的變化規律,可采用圖 6所示的等效電路對交流阻抗數據進行擬合,其中L表示感抗;Rs為歐姆阻抗,包括電池的電解液、隔膜、集流體及其與正負極界麵的阻抗等;Rct為由電荷傳遞作用產生的電化學阻抗,包括正負極的電極反應阻抗;Qdl代表電極反應的界麵電容;CPE為常相角元件,表示電荷擴散阻抗的常相位角元件.
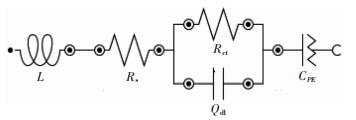 |
| 圖 6 LiFePO4電池的等效電路Fig. 6 Equivalent circuit of LiFePO4 battery |
通過圖 6的等效電路模擬,電池在不同放電倍率循環下不同循環次數的歐姆阻抗(Rs)及電化學阻抗(Rct)變化情況如圖 7和圖 8所示.在循環前期,歐姆內阻迅速減小,100次循環後又逐漸增大,由此表明,電池循環的前期是一個內部活化的階段,電池內部的各組分處於調整過程,包括電解液滲入電極內部、活性材料的均勻分布和電極結構的空間排列緊湊等,這些因素共同導致電池歐姆內阻的減小.繼續循環,電池內部副反應增多,導致電解液逐漸被消耗.另外,電極材料在反複充放電過程中使電極結構變得疏鬆或者SEI膜的破壞等,均有可能增大電池歐姆阻抗.電池循環前期,Rct的值先迅速減小,100次循環後逐漸趨於穩定,但200次循環後又逐漸增加,這一結果與歐姆內阻的變化規律基本相近,隨著電池循環前期的活化,電極活性材料的結構將更適宜鋰離子脫嵌過程,正負極的電極反應更易發生.循環繼續進行,電池的內部結構又逐漸劣化,使鋰離子在電池內部脫嵌的難度增大,造成電池的電化學阻抗增加.整個循環過程中,電池的歐姆阻抗和電化學阻抗都隨著循環次數的增加遵循先減小後增大的規律,這也與容量分析的結果一致.
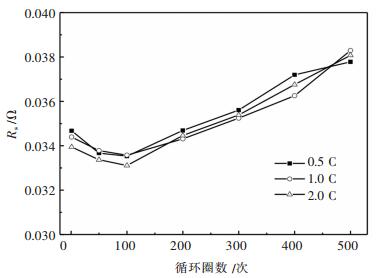 |
| 圖 7 不同放電倍率下不同循環次數的RsFig. 7 Rs of different cycles at different discharge rates |
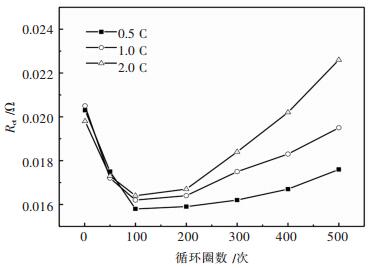 |
| 圖 8 不同放電倍率下不同循環次數的RctFig. 8 Rct of different cycles at different discharge rates |
通過圖 7和圖 8比較可知,不同放電倍率下循環得到的歐姆阻抗變化趨勢基本一致,但電化學阻抗的變化情況受放電倍率影響很大,在充放電前期主要受電池的活化作用影響,因此電化學阻抗在各放電倍率下變化基本一致,但隨著電池內部結構充分活化之後,放電倍率對電化學阻抗的影響較大,且倍率越高,電池的電化學阻抗增加越快.這一現象表明,放電倍率對電池的電極極化作用影響較大,而對電池內部結構的改變影響較小.
圖 9所示為電池處於不同放電倍率不同循環周期的歐姆阻抗與電化學阻抗加和得到的電池阻抗(Rtol)曲線.可知,在整個500次循環中,電池內阻在循環前期先快速下降,繼續循環後又逐漸增加.放電倍率對電池內阻的影響主要集中在電池衰退階段,而在循環的活化階段影響較小.
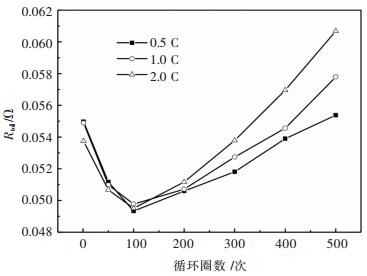 |
| 圖 9 不同倍率下不同循環次數的Rtol曲線Fig. 9 Rtol of different cycles at different discharge rates |
2.4 不同倍率循環的電池開路電壓變化
電池開路電壓(Open circuit voltage, OCV)是指電池處於未接負載的開路狀態時電池兩極的端電壓,是反映電池基本性能的重要特性. 圖 10所示為電池在不同放電倍率循環後電池處於放電態下靜置12 h後測得的開路電壓曲線.從曲線上可以看出,電池在前100次循環時開路電壓緩慢減小,100次到200次開路電壓迅速下降,200次後電池開路電壓基本保持不變,400次後電池的開路電壓又開始快速下降.這一變化趨勢表明,在循環前期(100次以內),電池開路電壓受循環次數的影響較小,這進一步驗證了電池循環前期是一個電池的活化過程.繼續循環,電池開路電壓呈現先快速下降再保持不變最後又快速下降的趨勢,這主要是由於在循環過程中正負極的結構發生改變以及活性鋰離子的損失而引起的.另外,比較圖 10中3組放電倍率下的開路電壓曲線可知,放電倍率對電池開路電壓的影響主要分布在循環400次以後,且放電倍率越高,開路電壓下降越快.
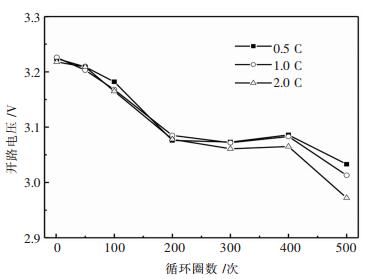 |
| 圖 10 不同放電倍率的開路電壓循環曲線Fig. 10 Open circuit voltage curve with different discharge rates |
圖 11所示為循環500次後不同放電倍率下測得的開路電壓與荷電狀態(SOC,state of charge)的關係曲線.由圖 11曲線可知,電池在循環500次後電池開路電壓隨電池荷電狀態的變化規律分成3個區段.當電池的SOC值低於0.3時,電池的開路電壓值變化較大,且SOC值越小,開路電壓值下降的越快;在0.3~0.9 SOC的中間區段,開路電壓曲線緩慢上升,電池開路電壓變化很小;SOC大於0.9時,電池開路電壓又快速升高.比較不同放電倍率下的電池開路電壓曲線可以發現,開路電壓會隨著放電倍率的增大而升高,但升高的幅度較小,也就是說,放電倍率對電池的開路電壓的影響很小,低倍率下電池的開路電壓較低.
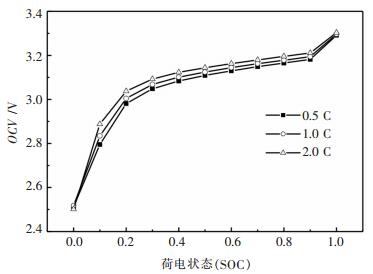 |
| 圖 11 循環500次後不同放電倍率下電池OCV-SOC曲線Fig. 11 Open circuit voltage curve with different discharge rates |
2.5 不同倍率循環的放電能量及熱量分析
鋰離子電池在放電循環過程中,一方麵需要向外部輸出電能,同時由於電池內部阻抗和電化學反應的存在也會產生熱能,這2部分的能量都是以化學能的形式儲存在電池內部,化學能的多少不僅跟電池內部各部件的材料結構與活性相關,還受溫度、充放電電流以及循環次數等影響. 圖 12(a)反映了電池在不同倍率下循環後測得的放電能量.由圖 12(a)可知,放電能量的變化規律,同容量變化趨勢基本一致,循環前100圈,不同放電倍率下的電池放電能量均增加,且所發出的能量基本相等.這說明在這一階段,電池的放電倍率對放電能量的影響較小,此時放電倍率不是放電能量的主要影響因素. 100圈循環之後,電池放出的能量會隨著循環次數的增加而逐漸下降,且不同放電倍率的能量下降速率不一樣,在高倍率下放電能量下降更快,此時放電倍率對電池循環放電能量的影響很大.
 |
| 圖 12 不同倍率下電池放電容量及熱量的循環關係曲線Fig. 12 Cycle diagram of battery discharge capacity and heat at different discharge rates |
鋰離子電池主要有4個熱量的來源:歐姆熱、電化學反應熱、極化熱以及副反應熱.一般而言,電池正常使用時,發生的副反應較少,並且充放電過程中,鋰離子電池的電化學反應熱較低,在計算總熱量時,可以忽略不計.鋰離子電池的歐姆熱是電池在充放電過程中由於電池內部的歐姆內阻在電流的作用下產生的熱量,其計算公式為:
| Qj=I2Rst | (3) |
式(3) 中:Qj為焦耳熱,J;I為充放電電流,A;t為充電時間,s;Rs為歐姆內阻,Ω.
極化熱計算公式:
| Qp=I2Rpt | (4) |
式(4) 中:Qp為極化熱,J;I為充放電電流,A;t為充電時間,s;Rp為極化內阻,Ω.
總熱量計算公式:
| Q=Qj+Qp | (5) |
式(5) 中:Q為總熱量,J.
將不同循環周期後的電池,通過直流脈衝法測量電池在不同放電深度下的直流阻抗.整個放電過程分為20個放電深度,每次放出5 %的電量,再以大電流對電池進行短時間恒流放電,根據該過程中電壓的變化計算出電池的直流歐姆內阻和直流極化內阻.當放電深度足夠小時,可認為其直流阻抗值近似恒定.以電池在不同放電深度下的直流歐姆阻抗和直流極化阻抗分別計算出電池處於不同SOC區間段內的歐姆熱和極化熱,將全部SOC區間段內的歐姆熱和極化熱分別加和,可得整個放電過程的焦耳熱與極化熱.
圖 12(b)、圖 12(c)和圖 12(d)分別是根據上述熱量公式計算得到的焦耳熱、極化熱以及總熱量的循環關係曲線.從圖 12中可知,在低倍率下,電池的焦耳熱、極化熱以及總熱量隨循環次數的增加基本保持不變,這是因為低倍率下循環時,放電電流較小,電池的極化程度低,對電池的內部結構影響較小,電池內部各阻抗值變化不大.增大電池放電倍率,放電電流增大,極化程度也加大,隨著循環次數增加,電池內部結構受到的影響加劇,電池內部的阻抗值也就逐漸增大,因此產熱也會逐漸增多.另外,在相同的循環次數下,大電流放電也會造成熱量增加,這會使電池內部溫度升高,電池的老化加快.
3 結論通過研究磷酸鐵鋰電池的不同放電倍率下容量、交流阻抗與開路電壓特性,得到了不同放電倍率循環下各特性的變化規律.
1) 磷酸鐵鋰電池的容量受放電倍率的影響較大,放電倍率越高,電池放出的容量越少,且電池放出容量與電池的放電倍率間滿足冪函數規律.
2) 不同倍率循環過程中電池放出容量隨循環次數的增加呈現先增後減的變化規律,電池在較高倍率下循環容量衰減更快,放電倍率對電池的循環放電容量的影響很大.
3) 循環過程中,放電倍率對電池歐姆內阻影響不大,而對電池的電化學阻抗影響明顯,在電池經過充分活化過後,放電倍率越高,電池的電化學阻抗增加越快.
4) 電池的開路電壓在循環後期受電池放電倍率的影響較大,且放電倍率越高,開路電壓下降越快.
5) 放電倍率與電池的放電能量以及熱量存在明顯的相關性,高倍率下電池放出的能量較少,熱量產生較多,老化速度加快,使用壽命降低.
電池在不同放電倍率條件下循環的容量、內阻和能量特性差別很大,因此,對電池的容量的估算要考慮倍率帶來的影響;電池在大電流條件下使用時易造成極化程度增加和電池內部材料老化加快;磷酸鐵鋰電池在高倍率下循環性更差;電池的開路電壓在不同循環階段受放電倍率影響程度不一.這些結論明確了磷酸鐵鋰電池的倍率循環性能特性,對電池的管理技術和壽命研究具有十分重要的意義.
| [1] | 韋連梅, 燕溪溪, 張素娜, 等. 鋰離子電池低溫電解液研究進展[J]. 儲能科學與技術, 2017, 6(1): 69–77. |
| [2] | SCROSATI B, GARCHE J. Lithium batteries:status, prospects and future[J]. Journal of Power Source, 2010, 195(9): 2419–2430. DOI: 10.1016/j.jpowsour.2009.11.048. |
| [3] | 段建鋒. 20Ah富鋰錳動力電池的性能研究[J]. 有色金屬科學與工程, 2013, 4(2): 37–41. |
| [4] | 趙世璽, 郭雙桃, 趙建偉, 等. 鋰離子電池低溫特性研究進展[J]. 矽酸鹽學報, 2016, 44(1): 19–28. |
| [5] | 孫豔霞, 周園, 申月, 等. 動力型鋰離子電池富鋰三元正極材料研究進展[J]. 化學通報, 2017, 80(1): 34–40. |
| [6] | 李恒, 張麗鵬, 於先進, 等. 鋰離子電池正極材料的研究進展[J]. 矽酸鹽通報, 2012, 31(6): 1486–1490. |
| [7] | 湯雁, 劉攀, 徐友龍, 等. 鋰離子正極材料的研究現狀與發展趨勢[J]. 電子元件與材料, 2014, 33(8): 1–6. |
| [8] | 閆金定. 鋰離子電池發展現狀及其前景分析[J]. 航空學報, 2014, 35(10): 2767–2775. |
| [9] | 楊見青, 關傑, 梁波, 等. 我國廢棄磷酸鐵鋰電池的資源化研究[J]. 環境工程, 2017, 35(2): 127–132. DOI: 10.11835/j.issn.1005-2909.2017.02.032. |
| [10] | 張克宇, 姚耀春. 鋰離子電池磷酸鐵鋰正極材料的研究進展[J]. 化工進展, 2015, 34(1): 166–171. |
| [11] | 劉冬生, 陳寶林. 磷酸鐵鋰電池特性的研究[J]. 河南科技學院學報, 2012, 40(1): 65–68. |
| [12] | 杜江, 張正富, 彭金輝, 等. 動力鋰離子電池正極材料磷酸鐵鋰的研究進展[J]. 新能源進展, 2013, 1(3): 263–268. |
| [13] | 郭紅霞, 喬月純, 穆培振, 等. 鋰離子電池正極材料研究與應用進展[J]. 無機鹽工業, 2016, 48(3): 5–8. |
| [14] | 詹世安, 湯寧平, 王建寬, 等. 磷酸鐵銼電池荷電狀態估算方法研究[J]. 無機鹽工業, 2015, 39(8): 1620–1624. |
| [15] | 李哲, 韓雪冰, 歐陽明高, 等. 動力型磷酸鐵鋰電池的溫度特性[J]. 機械工程學, 2011, 47(18): 115–120. |
| [16] | 匡勇, 劉霞, 錢振, 等. 鋰離子電池產熱特性理論模型研究進展[J]. 儲能科學與技術, 2015, 4(6): 599–608. |
| [17] | 李海英, 賈永麗, 張丹, 等. 動力磷酸鐵鋰電池產熱特性研究[J]. 電源技術, 2016, 140(5): 968–971. |
| [18] | MARTIN-MARTIN L, GASTELURRUTIA J, NIETO N, et al. Modeling based on design of thermal management systems for vertical elevation applications powered by lithium-ion batteries[J]. Applied Thermal Engineering, 2016, 102(5): 1081–1094. |
| [19] | 許守平, 侯朝勇, 胡娟, 等. 儲能用鋰離子電池管理係統研究[J]. 電網與清潔能源, 2014, 30(5): 70–78. |
| [20] | PEUKERT W. ǖber die Abhängigkeit der Kapacität von der Entladestromstärcke beiBeiakkumulatoren[J]. Elektrotechnische Zeitschrift, 1897, 20: 20–21. |
DIY 300AH: https://www.youtube.com/watch?v=HQZtyByhgMM
電容式主動均衡板原理:https://zhuanlan.zhihu.com/p/362671998
本文要求鐵鋰放電不低於2.5V,充電不高於3.55V:https://www.evworks.com.au/page/technical-information/lifepo4-care-guide-looking-after-your-lithium-batt/#:~:text=In%20the%20case%20of%20LiFePO4,3.5V%20and%204.2V.
10大廠家:https://www.lifepo4-battery.com/News/10-Largest-BATTERY.html








