東京大學研究生院教授片岡一則(Kazunori Kataoka)率領的研究小組日前宣布,開發出了一種能夠準確狙擊癌細胞的納米膠囊。
6月22日,一則“專殺癌細胞的納米膠囊被研發出來”的消息引發關注。
新華社報道稱,東京大學研究生院教授片岡一則(Kazunori Kataoka)率領的研究小組日前宣布,開發出了一種能夠準確狙擊癌細胞的納米膠囊,幾乎不傷害正常組織,研究小組準備經過臨床實驗,最快在5年內使這一技術達到實用化。
這一納米膠囊被網友評論為曠世奇藥,更有網友稱,“我看到一個諾貝爾獎!”
那麽,業內專家怎麽看?
武警廣東省總隊醫院原腫瘤內科主任謝強告訴澎湃新聞(www.thepaper.cn),該納米膠囊的治療方法本質上是放療——利用γ(伽馬)射線殺死癌細胞,使癌組織減小,該療法的確具有臨床應用價值,但
不是這樣癌症就治愈了,或根治了,仍要考慮腫瘤的複發和轉移等問題,而腫瘤的複發和轉移是很多癌症患者放療之後仍然麵臨的難題。
該醫院腫瘤內科副主任醫師宋曉軍也告訴澎湃新聞,目前還沒有一種放療方法能保證根治癌症。
中國科技大學高分子科學與工程係副教授葛治伸2010年11月到2012年3月曾在東京大學做博士後,研究方向為“多功能聚氨基酸嵌段聚合物的合成及其在腫瘤基因治療上的應用”,導師正是片岡一則。
葛治伸表示,該納米膠囊相關理論方法——納米材料本身的特性、腫瘤放療、以及影像學的手段——都已經應用了多年,但此前沒有聯合使用過,“聯合使用”是該研究的巧妙和創新之處。但需要注意的是,目前該納米膠囊隻做了小鼠實驗,臨床實驗還未進行,距離真正應用,尚需相當時間。在人體上是否有效,有多大效果,還不知道。
上海交通大學納米生物醫學工程研究所所長、納米重大科學研究計劃(“973”)項目首席科學家崔大祥告訴澎湃新聞,這是一種新的治療方法,值得嚐試,但能否臨床應用,還有很多研究工作要做。此外,產生熱中子輻射的設備很昂貴,而製備的納米膠囊無腫瘤靶向性,也可進入肝髒等其它部位,這些都是挑戰性的難題,不易解決,離臨床應用,還有一定距離。
新華社報道稱,片岡一則指出:“開腹手術需要住院將近1個月,利用這種膠囊,有望實現癌症治療當天就能回家。”
而謝強認為,
放療都可以當天治療,當天回家,這是放療的特點。
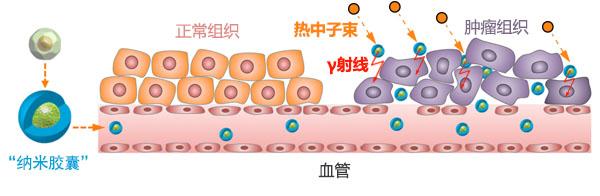
片岡一則實驗室“納米膠囊”的抗癌原理圖。
片岡一則實驗室該研究的論文6月11日在線發表在學術期刊《ACS NANO》(American Chemical Society Nanoscience,美國化學學會-納米科學)的網站上,論文題目為《利用磷酸鈣與釓螯合物的雜合膠團進行影像學示蹤的腫瘤的釓中子俘獲療法》(Hybrid Calcium Phosphate-Polymeric Micelles Incorporating Gadolinium Chelates for Imaging-Guided Gadolinium Neutron Capture Tumor Therapy)。
論文顯示,釓中子俘獲療法(GdNCT,Gadolinium Neutron Capture Tumor Therapy)是中子俘獲療法(NCT)的一種。
事實上,60年前,中子俘獲療法已經在臨床中使用。
中國工程院院士周永茂2009年發表的論文《一種二元放療靶向治癌的新技術——中子俘獲療法(NCT)與醫院中子照射器( IHNI)》顯示,1951年,美國神經外科醫師W.H.Sweet等人進行了人類首次硼中子俘獲療法(BNCT)的臨床試用。
與硼中子俘獲療法不同的是,片岡一則實驗室,將硼更換成了釓,而成為GdNCT。原因是Gd吸收熱中子後,輻射出的γ射線比α射線的殺傷力更強。其次,Gd的螯合物——Gd-DTPA經常被用作磁共振成像(MRI,magnetic resonance imaging)的增強劑,可以改善成像的效果,更精準地定位。
為什麽納米膠囊能夠狙擊腫瘤細胞?葛治伸解釋說,納米尺度的膠團一般都會選擇性地富集在實體瘤組織中,這是納米材料的特性,但這僅限於實體瘤,如果腫瘤細胞擴散了呢?

 選擇“Disable on www.wenxuecity.com”
選擇“Disable on www.wenxuecity.com”
 選擇“don't run on pages on this domain”
選擇“don't run on pages on this domain”