雅美之途
教育,人文,社會
中國艾博公司做出的新冠mRNA疫苗,隨著劑量增加抗體滴度不升反降。更要命的是,疫苗劑量增加時誌願者的發熱反應還增加。
最近與國內專業人士通訊,證實了我當時第一時間在文章中對國產mRNA疫苗不行原因的推測。那就是他們隻懂生化而不暗免疫學,打進去的mRNA很多被免疫係統作為外源物排斥掉了,人體也因為異物的侵入而發高燒。
這真是中國之殤,搞成現在國家成為世界之奇葩,隻有封城一條路。中國mRNA疫苗研究者以為可以糊弄老百姓,彎道超車。上層的人士又不懂,造成現在疫情曝發的第三個年頭仍然十分困難。中國應該也有做免疫不錯的海歸科學家,他們怎麽不教教工業界的人士?不過這也怪美國人,沒有把艾博的海歸總裁訓練好。
福奇在疫情的極早期就將睹注壓在Moderna的mRNA疫苗上。盡管mRNA疫苗的理論與實踐在美國開創,但是他能拍板讓NIH為Moderna疫苗做臨床試驗,這是需要非凡的膽略的,當時新冠剛剛從武漢傳到美國西雅圖。盡管那麽多攻擊托尼的保守派朋友,但是我始終認為福奇是美國和世界抗疫的第一大功臣。
我們知道隻要一點就可能讓福奇與Moderna的決策失敗,那就是新冠除了ACE2受體外還有第二個重要受體,北大教授鄧宏槐在NYU發現了艾滋病毒的輔助受體CCR5。因為mRNA疫苗隻設計了封閉ACE2受體的序列,病毒可以擺脫疫苗刺激的抗體封鎖,從其他途經進入細胞。慶幸的是,中國西安科學家當時報道的新冠利用CD147作為輔助受體的結論沒有被重複。
中國落到隻有全民核酸和封城這局麵的很重要原因是科學家的集體腐敗,他們麵對香港出現科興疫苗98%防重症和死亡的可疑數據時都很少人出來糾錯。有些科學家不僅沒有水準,更沒有擔當,他們隻會吹牛。
國家投入大量資金在科研上,當薩斯出現時, 中國院士弄出薩斯病毒是支原體的國際笑話。現在中國科學家隻有本事任新冠肆虐隻能讓上海和北京人民受苦,他們卻拿足夠資助研究同性戀果蠅的打架。
中國基本上沒有策略,開始以政治手段鼓勵滅活疫苗公司黑全球先進的mRNA疫苗。看見mRNA疫苗有成效後,他們又走向另一個極端。風投公司不懂行,不去評價一位海歸的公司的技術儲備就下高達10億美元的單去投資,中國大陸真是人傻錢多。
沒有真正的免疫學家在他們公司把關,讓他們在疫苗不加修飾的核苷酸時上馬疫苗,他們的膽子太到令人難以置信的程度。麵對這樣的失敗,他們的辯稱是他們的專利裏沒有修飾的核苷酸這一項,那些專利局也盡是些糊塗人士,其實根本的原因遠不止於此。
我們對複印機旁的UPenn科學家Katie Kariko和Drew Weissman的傳奇對話應該很熟悉了,讓我再講講。Kariko在幾輪老板離開去工業界後麵臨職業選擇,年輕的助理教授Weissman希望她能加入自己研究組做艾滋病疫苗,Weissman是福奇實驗室訓練出來的。
Kariko會在培養係統中製備mRNA,但是這些mRNA打到老鼠體內後不能有效製備出蛋白質。不僅如此,注入mRNA後老鼠會出現免疫應激反應,諸如皮膚皺褶,舵背,最後不吃東西或停止奔跑,老鼠病了。
他們開始也不清楚,隨後才發現是機體內存在的識別核酸的TLR將他們人工合成mRNA作為異物打擊,就像攻擊病原體那樣的免疫攻擊,具體機製可讀我以前的文章。
他們注意到tRNA含有大量的所謂假尿苷(Pseudouridine), 為尿苷被異構化的產物。這些假尿苷可以防止RNA被免疫係統排斥,這是他們能完成生物功能的前提。其實在漫長的進化過程中,為了生存,我們哺乳動物的核酸裏的很多核苷酸都是經過自我修飾的。最常見的修飾方式就是在核苷酸裏加上甲基,也就是所謂的甲基化。
這樣我們的免疫係統就不會隨便打擊我們體內非常重要的核酸-DNA和RNA, 也就是我們經常說的免疫係統對自身組織的耐受性。如果這種耐受性被破壞了,我們就會得自身免疫性疾病。大家知道的係統性紅斑狼瘡的一個機理,就是因為有些病人的DNA沒有被有效地甲基化,處於原因不明的低甲基化狀態,這樣促使人體產生了抗DNA的自身抗體。這些抗DNA的自身抗體是狼瘡的診斷標準,為聖路易斯華大前華裔教授Eng Tan在洛克菲勒發現的。
細菌和病毒的核苷酸被修飾的程度遠比哺乳動物的核苷酸低,這又讓我們回到免疫係統的根本功能之一,那就是識別自己和異己。我們的免疫係統將沒有被修佈的病原微生物核苷酸作為異己打擊,而對自己被修佈過的核苷酸則不產生免疫反應。
當Kariko和Weissman認識到這點後,他們在體外轉錄實驗合成mRNA時加了各種甲基化或異構化等修飾的核苷酸,當他們再將這些含有修飾核苷酸的mRNA打入機體後,老鼠沒有產生免疫排斥。
他們很簡單的實驗,一個體外轉錄實驗,但是沒有想到能夠徹底改變了新冠疫情。諾貝爾獎幾乎肯定會授予Kariko和Weissman,時間問題,美國拉斯卡和加拿大Gairdner這些前期獎項都授予了他們。授予諾貝爾獎金的原因就是他們發現了防止免疫係統攻擊mRNA的途徑,為mRNA治療開辟了道路。
他們的Immunity論文是在2005年發表的,當時的編輯部己經從聖路易斯華大(從1997年開始的)轉到耶魯和NIH。評審專家很顯然識貨,在同意發表時還安排了評述。
美國的厲害是世界一流的地方到處都是,比方說UPenn科學家使用的修飾核苷酸(m5C, m6A, m5U, Pseudouridine或2#-O-methyl-U)來自聖地亞哥的小公司TriLink,為業界的世界領袖。
中國公司見勢不妙,也隻補申了Pseudouridine的專利。我估計他們現在還是得不到工業化程度的其他修飾核苷酸,所以隻有硬性創關mRNA疫苗造成現在的失敗。作為背景資料,輝瑞和Moderna疫苗都使用了修佈核苷酸。
什麽叫卡脖子?這就是,一點小的修飾核苷酸就可以讓你苦不堪言。當然這在經貿正常的情況下可以很容易購買,所以還是外交出了大問題,中國走到了一條與現代世界文明對抗的路。如果美國禁運,導彈會失準,飛機都可能掉下來。
我估計中國公司再怎麽也應該讀過2005年的Immunity論文,懂些原理,還是技不如人。在這種情況下,隻有二條路可以走:迅速批準複必泰疫苗,以及允許mRNA疫苗進口中國。這也沒有什麽麵子可丟的,英國在自己製備不出mRNA疫苗的情況下,批準輝瑞疫苗比美國還早。
現在分享我在22年1月和20年12月的兩篇相關文章,看我在第一時間說了什麽,讀者也可以了解一些科學研究過程。
中國首款mRNA疫苗的效果不理想 (2022-01-27 21:31:32)-雅美之途
這是中國首款mRNA疫苗臨床試驗的一期結果,來自艾博公司,發表在《柳葉刀》上,應該是問題不小。艾博公司的25微克的劑量100%發燒,還不是一般的燒。在他們的臨床一期試驗文章中,在25微克這個低於輝瑞30微克的劑量裏,88%的接種人達到三級高燒,在38.5-39.5度之間,這是麵對大眾不能接受的嚴重副作用。我開始以為這恐怕是脂質包層不過關造成的,其實不僅是這些。
艾博25微克刺激的抗體目測大概隻有恢複期抗體的80%,雖然比科興高一倍,但是我們不應該對三期報希望了。艾博mRNA疫苗的15微克達到刺激抗體的高峰,25微克還下降,不明白這是為什麽?輝瑞是30微克,遠沒有這麽多發高燒的,Moderna的100微克也沒有,他們的疫苗都達到恢複期抗體的3.8-4倍。
我也是在柳葉刀看見科興隻有40%恢複期抗體後覺得滅活疫苗不行的,現在不幸被我猜對。UCLA的吳尊友校友最近終於說了實話,中國現在的突破感染率很高,107例感染,106打過滅活疫苗至少二針,有些還打了加強針。雖然麵對絕大多數打了疫苗的人群,這是數學規律,但是滅活疫苗也太不給力了。
我們覺得艾博可能是使用的原始株的序列,因為他們去年就上了臨床試驗,最多考慮了D614G突變株。現在輝瑞疫苗麵對奧密克戎的保護力也隻有60-70%,如果艾博麵對奧密克戎做臨床三期,恐怕保護力也就是50%左右,那將會是令人失望的。中國應該拋棄偏見迅速批準複必泰,至少輝瑞加強針對奧密克戎可以有80-90%的保護力。
英博從複旦去Northeastern University 讀的PhD,在波士頓藥廠工作數年後於三年前回國創辦艾博,中國對他報以厚望,並且不惜代價壓住複星的複必泰不批。艾博和複星成了複旦人的競爭,歸根結底還是得益於美國,複星高官敲定BioNTech都是在波士頓。
麵對媒體的質疑,艾博創始人英博的回複令人失望,避重就輕想過關。英博居然這樣透露還沒揭盲的臨床三期:“雖然目前還未揭盲,數據還未收集完整,但舉一組收到的盲態數據為例,海外III期臨床盲態下的2149個案例裏三級發熱患者比例僅有個位數“。他以“盲態”的概念糊弄我們大眾,我不知道是否合法,但是這樣麵對媒體十分不妥,讓人覺得幾乎將臨床試驗當兒戲。
據我獲得的一個很重要的消息,那就是他們的疫苗沒有修飾核苷酸。如果這是真的,可以解釋很多結果。因為疫苗很難突破TLR的識別與免疫排斥,不僅發燒還會造成疫苗抗原性的丟失。劑量越高排斥越強,所以抗體滴度不升反降。副作用隨劑量增加而增加,抗體滴度隨劑量增加而降低,這個可能通過不了中國藥檢。
鑒於mRNA疫苗最低劑量的輝瑞都是30微克,Moderna為100微克,我甚至大膽猜測,艾博將最高劑量定在25微克可能是因為再高的劑量所出現的副作用讓他們受不了。他們將在後期臨床試驗將劑量進一步降到5,10和15微克,明顯是在25微克遇到了困難。他們量效結果是遞減的,其實25微克都有排斥反應出現,因為他們沒有修飾核苷酸。
艾博疫苗設計時隻是針對RBD?麵對突變株四起的今天他們也太大膽了,輝瑞麵對原始株都是放的全段S蛋白的核酸。艾博疫苗導致淋巴細胞下降可以理解,但是應該是暫時的,並且在6-8天恢複正常。
這裏的科學積累是很難彎道超車的,很多東西打摸就是幾年,工業化量產更是談何容易。Moderna受UPenn科學家工作的鼓舞創辦也好多年了,Kariko和Weissman的Immunity paper是在2005年發表的,他們奠定的避免機體排斥的原理使輝瑞和Moderna都修飾了疫苗的核苷酸。MIT Robert Langer做脂質delivery也很久了,艾博與美國的差距很大,這顆衛星靠海歸隻有三年的人放不可靠,雖然是美國訓練出來的人主導的。如果我能給建議,中國不應該對艾博疫苗報太大希望,而是需要迅速批準複必泰,然後猛攻複星的高質量產能瓶頸。
新冠mRNA疫苗:背後的英雄和他們的故事 (2020-12-04 11:37:59)-雅美之途
美國輝瑞mRNA疫苗最近的好消息,讓我們把注意力都集中在土耳其裔德國夫婦所創辦的小生物技術公司BioNtech,以及他們對新冠mRNA疫苗的貢獻,他們無論從金錢和榮譽上都得到了豐厚的回報。BioNtech總裁Ugur Sahin的野心很足,他要將自己創辦的德國公司變成類似美國Amgen或Genentech這樣的生物科技公司。那他還有很長的路需要走,因為德國缺乏美國這種鼓勵創新的土壤。
實施這些mRNA疫苗是科學的應用階段,新冠疫苗將mRNA治療提前了好多年,BioNtech以前的mRNA技術是為了癌症治療的,做新冠幾乎他們連夜的轉向。他們長久的課題是通過生物信息學的努力找到與MHC結合的癌細胞抗原,然後通過mRNA去合成這些抗原,注入到機體希望產生抗癌免疫力,也就是所謂腫瘤疫苗的概念。
但是無論是癌症mRNA的治療也好,還是mRNA新冠疫苗也罷,它們都是需要很原始的科學創新才能推動的,而這些基礎原創性科學來源於美國常春藤盟校之一的賓大醫學院的Katalin Karikó 和Drew Weissman,一個匈牙利裔科學家和一個美國猶太醫生的工作。我們可以毫不誇張地說,他們奠定了mRNA疫苗的科學基礎,沒有他們的貢獻就沒有BioNtech和Moderna的mRNA疫苗。我在以前博文中隻提過一句這些背景就被讀者問及,當時沒有展開,今天過節在家可以花點時間多聊聊。mRNA應用到大鼠裏在1990年就在威斯康辛大學通過實驗完成,而應用到體內表達蛋白質則可追溯到1992年,但是mRNA遭遇免疫排斥的挑戰始終困擾著科學家。
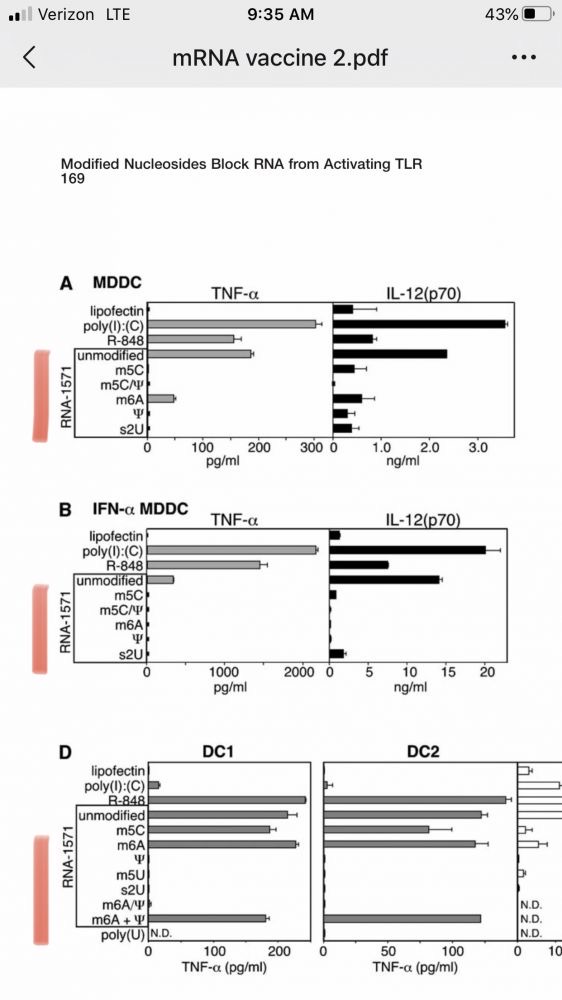
我們可以追查到他們在2005年的革命性的Immunity論文,當時50歲的Katalin Kariko作為第一作者,Weissman為資深作者。為了便於大家閱讀理解,我特別對有意義的部分標出了紅線。為避免機體的免疫排斥反應,他們在轉錄過程中加入堿基甲基化或其他修飾後的核苷酸,然後測試發現mRNA的免疫原性消失了,這些稍微修飾的mRNA不能刺激機體產生細胞因子和活化樹突狀細胞。這是人類第一次實現了注射mRNA不刺激免疫反應而遭遇排斥的後果,這是所有mRNA治療和mRNA疫苗的起點。
她們做這個實驗的前提是,如果DNA含有沒有甲基化的堿基能夠刺激機體的TLR9受體產生免疫反應,但是如果DNA被甲基化了它就不能刺激機體產生抗體。眾多科學家包括我涉及的工作在內,認為TLR9的缺陷與自身免疫性疾病相關。她們也知道雙鏈和單鏈RNA分別能活化TLR3和TLR7,以此自然想到將mRNA人為地甲基化能夠防止它們被免疫係統排斥掉。這裏又出現了進化壓力在人體免疫中的效應,因為人體自身RNA的甲基化程度比細菌的RNA要高十倍,這樣TLR便有效地擁有二個生物學功能:有效地幫助免疫係統識別那些低甲基化的細菌,對自己身體內的高甲基化的RNA則無反應,這樣可以避免自身免疫性疾病的產生。
Katalin Kariko在30歲才從匈牙利到美國尋求職業的機會,帶著幼年的女兒,也像我們當年那樣隻有幾百塊錢來美國打天下。這女兒後來也讀了賓大,參加賓大的皮滑艇隊,並且代表美國得過北京和倫敦奧運會的兩枚金牌。Kariko在美國的首站是費城的Temple大學,後來轉到了賓大。當時她在賓大的教授職位不能提升,因為拿不到資助,老公在匈牙利的簽證也成問題,自己好像還有癌症問題。她完全拿不到資助,這種情況在美國名牌大學所麵臨的隻有兩個命運,要麽離開,要麽降職,她選擇了後者。她很幸運的是找到與猶太醫生Drew Weissman合作的機會,醫生科學家往往比較容易弄到研究經費,但是Weissman對她的課題感興趣。
他們後麵還有係列文章研究這些修佈的mRNA在體內的命運,發現它們不能刺激機體產生細胞因子等免疫反應外,這些mRNA在進入機體後仍然保留合成蛋白質的功能。當然後麵也有人應用HPLC等別的方法以避免mRNA的免疫原性。Moderna公司的創辦人哈佛教授Derrick Rossi稱Katalin Kariko和Drew Weissman應該分享諾貝爾化學獎,Rossi被這個工作折服的最重要的原因是他應用修佈後的RNA能夠使體細胞重新編程為幹細胞,這也是他和Tim Springer,Ken Chien和Robert Langer共同創辦Moderna的原始動機。Rossi最後被排擠出了Moderna,這故事有點複雜,我們這裏從略,喬布什也有被蘋果踢出去的經曆。雖然Katalin Kariko現在是德國BioNtech的SVP,但是別忘了這玩意是在美國發明的,她在賓大的25年時光還為女兒收獲兩枚奧運會金牌創造了條件。
免疫係統有DNA和RNA的識別感應器,授予過諾貝爾獎的TLR為其中之一,Kariko和Weissman在文中正是應用的TLR識別外源性mRNA的功能。Toll-like receptors (TLRs)作為受體能識別機體的構建磚塊,像核酸片段和小脂質成份,從這些小磚塊進而識別誰是外源或內源的,為免疫係統預警或誘發免疫反應。這個在學術上叫pattern-recognizing receptors, 為耶魯教授Charlie Janeway 從腦袋裏想出來的,他認為人體中存在固有的這些受體隨時準備迎接這些廣泛的外源性抗原,後來他們共同發現了TLRs。生物醫學不像物理學那樣存在理論生物學,如果有的話,Charlie Janeway就是罕見的一位。生物醫學的任何事情都必須有牢固可靠的證據,但是Janeway在1989年的冷泉港評述論文中,硬是假設出了免疫係統擁有識別內外源Patterns的蛋白,像Paul Ehrlich創立抗體側鏈學說那般,堪稱天才。Janeway為哈佛畢業生,出身於醫學世家。他當時從NIH完成受訓後專選耶魯去做教授,因為他覺得那裏的免疫學薄弱,現在耶魯與哈佛和聖路易斯華大列為美國最厲害的三大免疫學重鎮。十分可惜的是,Charlie Janeway於2003年在60歲的事業黃金時段英年早逝。如果他活到頒發TLR諾貝爾獎的2011年,諾貝爾委員會再怎麽也不會錯過他的。
這裏簡單談談為什麽耶魯大牌免疫學教授Ruslan Metzhitov與TLR的諾貝爾獎無緣?為什麽諾貝爾獎公布後引來耶魯眾多世界級別的免疫學家聯合署名在Nature發表文章抗議?
與TLR相關的現象是在與德國交界的法國Strasbourg發現的,Jules Hoffmann實驗室。Strasbourg為德國名字的法國城市,從中可以看出法國和普魯士多次在此城市上的易手,現在為歐盟的議會所在地。雖然後來那篇1996年的Cell論文的第一作者出來公開翻臉,稱Hoffman僅是實驗室的老板,他其實沒有太多的貢獻。他們發現果蠅中的有些Toll突變型特別容易被細菌和真菌感染,所以他們推測Toll可能與固有的免疫防禦功能有關。
Toll這個專業單詞來自一位德國女性諾貝爾獎胚胎學家,為德文裏驚歎的意思。Ruslan Metzhitov來自前蘇聯加盟共和國烏茲別克,他在莫斯科讀博士時就受到了Janeway文章的鼓舞。當時他在莫斯科大學的所在係每月的預算隻有$20美元。在1990年,Ruslan仍然使用400位教職員工和學生共享的電郵係統與Janeway通訊,為了節約經費,每人隻能寫300個字。Ruslan Metzhitov麵對的挑戰遠勝過我們當時的中國,當時隻有蘇聯國家自然科學院有原版的Nature和Science, 每期傳閱後回圖書館都被磨損得厲害。他們還不讓普通人員隨便進入外文圖書館,Ruslan隻有靠嘴甜才能混進去。當時他為了複印Janeway的文章,耗去他每月二美元生活費用的一半,這就是我通常說的對科學的Passion。
Janeway跟太太說:“有位十分聰明的俄羅斯人想入我的實驗室”,他太太開始完全不相信這種可能性的存在。Ruslan最終抵達美國,他在UCSD短暫停留後前往耶魯。受Janeway假設的鼓舞,Metzhitov和Janeway在1997年在Nature上發現了首個Toll-like receptor-TLR4, 他們後續還克隆了好幾種TLRs。Janeway去世後,Metzhitov是世界範圍內在TLR領域貢獻最大的科學家。
西南醫學中心的Bruce Beutler在1998年的Science文章中發現,TLR4就是我們熟知的革蘭氏陰性細菌的細胞壁上存在的內毒素(LPS)的受體。他們在動物實驗中非常漂亮地證明,TLR4缺陷的老鼠能夠扺抗大劑量LPS誘導的休克。LPS為一種脂多糖,因為它是強大的免疫刺激劑而讓做生物藥物的人經常頭痛。
在TLR諾貝爾獎頒發的2011年, Ruslan Metzhitov早己不是博後,而是HHMI研究員和耶魯教授,譽滿全球的免疫學家。當然Ruslan與Janeway發現係列TLRs時還隻是博後,這裏可看我以前提出的導師與學生分享諾貝爾獎的三項原則之一:應該是隻有自己研究組的原創,沒有來自外校的競爭。這裏Ruslan Metzhitov的氣憤可想而知,他曾經在一個報告會議上控訴,有人為了榮譽甚至不惜更改Charlie Janeway的Wiki網頁,這是不點名的指控Bruce Beutler。耶魯與西南兩邊基本鬧翻了,TLR4是耶魯人發現的,西南人發現它是LPS的受體,誰重誰輕大家自己看吧。Ruslan的妻子是日裔美國院士Akiko Iwasaki,現在病毒免疫領域如日中天的人物。前不久北大羅金才教授領導的研究組發表的關於腦淋巴係統與癌症關係的論文,與Akiko Iwasaki形成了直接的競爭,相互重複了各自的結果。
那次諾貝爾獎如果僅授予TLR會最公平,讓Jules Hoffmann,Ruslan Metzhitov和Bruce Beutler分享,應該皆大歡喜。但是諾貝爾委員會硬要在那年加入發現DC的Ralph Steinman, 這位洛克菲勒教授在頒獎前三天去世了。他的發現也是在博後期間完成的,更老的猶太導師早就去世幾十年了。Steinman是阿肯森在麻省總院時的總住院生,阿肯森的直接上級醫生,他們一起結伴訪問過日本,Steinman也是神童Bruce Beutler的博後導師。
總之,2011年的諾貝爾醫學獎充滿傳奇,法國和美國的研究組都出現了指名道姓的發現權之爭。諾貝爾獎也開創了授予去世者的先例,他們是否應該為牛頓、伽利略和達爾文補發諾貝爾獎呢?mRNA的根基是在美國奠定的,通過純的科學興趣所驅動,當然需要匈牙利裔科學家的頑強和烏茲別克裔科學家的智慧。造就這些科學創造的主要原因是因為美國自由的研究環境,這是很多世界大國無法企及的東西。你如果禁固了人們的思想,就別奢望什麽科學的創造。美國仍然像一塊磁鐵石般,吸引著來自世界各個角落的才子佳人。






宰相肚裏能撐船。您是終身教授,還怕啥?好多人把罵自己的貼置頂。