今天朋友在群裏分享了這篇Cell論文,證明新冠病人不僅存在中和抗體,也產生一係列能夠增強新冠感染力的抗體。這類抗體在新冠重症感染的病人中更多,這就是我們通常所說的ADE (Antibody-dependent enhancement,抗體依賴性病毒增強效應)。 初看文章題目發覺就是我曾經介紹過的日本大阪大學的工作,當時我的博文隻發表在以前的公眾號上,在文學城上沒有。因為受歡迎,我的文章的盜版很多。這次也確實能從其他網站找到,似乎應該感謝偷文章的人,大家可以對照看附後的博文。 另外告訴大家一個新的進展,雖然我的公眾號仍然在服無期徒刑,但是他們最近允許整體打包將以前的文章下載。 我們都希望自己居住的地區達到群體免疫,美國舊金山地區因為打了足夠的高質量疫苗恐怕已經達到。沒有群體免疫所形成的免疫牆,接種疫苗後我們再次遇見新冠病毒是經常的事,我們能夠健康是因為疫苗所誘導產生的抗體能夠將病毒迅速消滅。現在的問題是自然感染與疫苗所刺激的抗體是否能夠幫助重新遇見的病毒更容易感染,當然必須是使病毒更容易進入細胞,然後繁殖和造成危害。 我時刻需要提醒同濟的美國微生物學家,最終應該是疫苗而不是隔離將帶我們走出疫情的悲慘世界。他是衛生係的畢業生,更加相信流行病學的所謂三板斧頭措施:發現傳染源,切斷傳染途經和保護易感人群。 這篇華裔第一作者的日本大阪大學實驗室的文章認為,那些新冠病人所產生的“增強抗體”通過提高新冠病毒的S蛋白與ACE2受體的結合而增加新冠病毒的感染力。這是我見到的首篇認為新冠感染存在ADE效應的實質報道,他們的預影本在網上已經存在了至少半年,Cell也審稿了超過四個月,領域對他們的謹慎應該是有目共睹的。 他們發現的“增強抗體”是通過與S蛋白的N-terminal domain (NTD)結合完成的,這個結合將RBD (受體結合域)的構象改變成開放型,從而增加了RBD與ACE2受體的結合。因為ACE2受體的表達到處都是,所以他們的發現如果是普遍現象,我們應該看到對單個病人或整個疫情的影響更重。但是我們在現實世界沒有見到新冠加重的趨勢,特別是在廣泛接種了疫苗的國家。他們除了實施過受體與配體結合的功能實驗,也通過結構生物學找到特異性的抗體結合位點。 新冠病毒的S蛋白有兩個亞基:S1和S2。S1負責病毒的吸附,S2的功能則是介導膜融合。我們知道蛋白質翻譯是從N端(NTD) 向C端(C結構域)推進的,病毒的RBD可能存在於NTD或C結構域。新冠病毒和MERS(中東冠狀病毒)的RBD在C結構域,小鼠的肝炎病毒的RBD則存在於NTD。日本大阪大學發現的是與登革等病毒很不同的ADE, 因為不是非中和抗體,這個是直接涉及中和抗原與病毒受體的結合,他們也看到自己的抗NTD的“增強抗體”能夠降低中和抗體的結合。那些中和抗體應該是通過自然感染產生的,因為當時疫苗還沒有廣泛使用,中和抗體與“增強抗體”產生的時間是什麽也不清楚。 通過輝瑞mRNA疫苗是否也能產生這類“增強抗體”,因為輝瑞疫苗是針對全長的S蛋白,不僅僅隻對RBD。如果我是論文的審稿員,我可能會建議他們測試那些突破感染的患者。 他們發現的這個ADE非常特別,不是我們通常知道的通過Fc受體或補體受體介導的。我從文章中沒有看出他們是如何排除這些受體的,各類Fc受體的表達比較廣譜,補體受體的表達相對窄些。這些抗體與NTD的結合是使RBD成開放構象的關鍵,但是他們看見沒有Fc端的抗體Fab段不能開放RBD,隻有完整的抗體(Fc和Fab)才行,他們怎麽能排除Fc受體呢?他們這樣聲稱排除了Fc受體的影響,至少應該做Fc受體的封閉實驗。 他們最不可思議的結論是發現在非感染人群中,也就是我們正常人中,也含有抗新冠S蛋白的NTD的增強抗體。那是怎麽產生的?通過交叉感染還是從天而降的? 這些“增強抗體”隻是針對S蛋白的,而不是傳統上導致ADE的非中和抗體。但是這不能證明mRNA疫苗比滅活疫苗更危險,我們還是應該依據龐大的群體免疫接種的效果判斷,看看以色列和英國漂亮的新冠病例曲線,他們沒有發現明顯的ADE。 美國如此大規模的開放,不戴口罩,新冠感染人數持續下降,所以這篇文章可能就是發現了新冠感染的一種特殊現象。  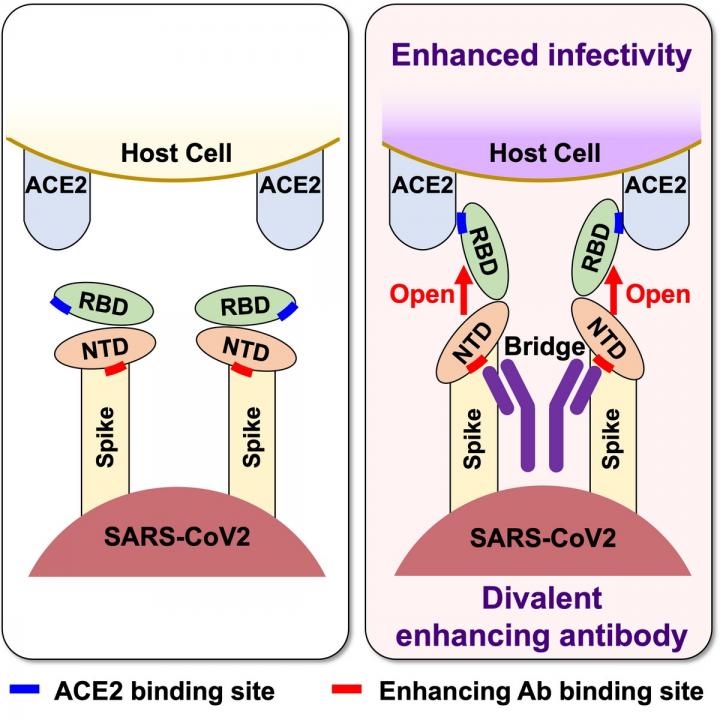 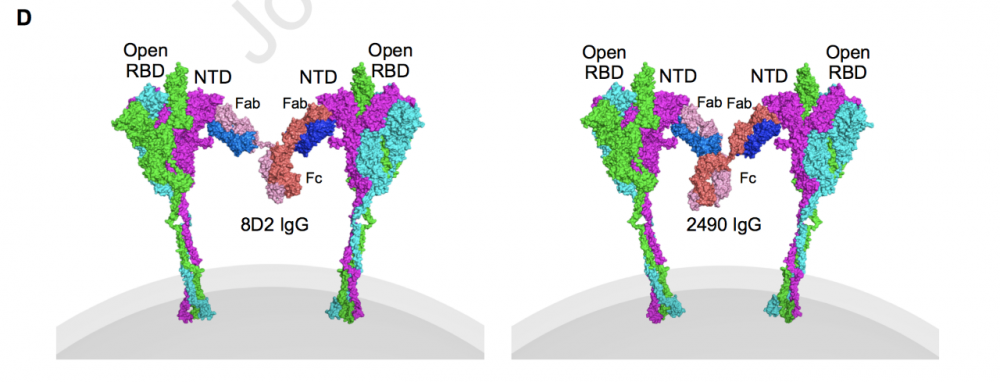
可以結合下麵我以前的文章綜合了解。 日本發現新冠病毒存在ADE,為新冠疫苗添憂 雅美之途;2021年1月4日 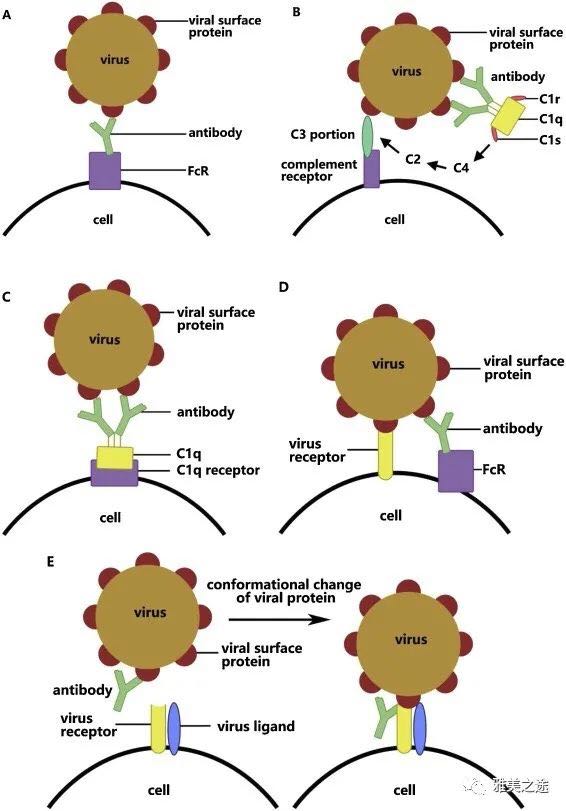
從網上借來的說明ADE(抗體依賴性病毒增強效應)的圖解。這個我喜歡,因為把我們研究的補體係統也涉及了。補體活化產物通過連接病毒和補體受體將病毒帶入細胞內,當然還有能與抗體結合的補體C1q受體。學術界始終存在Fc受體與補體受體誰更重要的爭寵之戰,每次總是Fc那幫家夥占上風,這位製圖科學家給了補體學家一些公道。 正文 我在上篇倍受歡迎的題為《mRNA疫苗優於滅活疫苗的免疫學基礎》的文章中說:“滅活疫苗也會刺激產生非中和性抗原的抗體,這些抗體容易讓人擔心產生抗體依賴性增強效應(ADE),使再次感染病毒時病情加重,現在還沒有在新冠中看到ADE”。 如今科學的進展飛速,尤其是關於新冠病毒的知識。現在有篇來自日本大阪大學的影印版論文證明,我的上麵這段話需要修正,因為他們確實發現了新冠病毒的ADE現象。這是對新冠病毒滅活疫苗的沉重一擊,讓我的心頭一緊。如果這工作被重複的活,後果相當令人擔憂。讀了他們的論文才發現,他們的工作甚至可能涉及到隻針對S蛋白的輝瑞和Moderna的mRNA疫苗,因為這個ADE是通過抗S蛋白的抗體實現的。 機體產生的抗體是讓我們抵抗病毒的,為什麽它們不幹好事還參與做幫助病毒的壞事?免疫係統做壞事的時候多著呢,阿肯森這位終生為自身免疫病人操心的醫生科學家甚至說,免疫係統最重要的功能是保護基因載體到17-18歲,以達到能夠傳基因的生殖年齡。他後麵的話沒有說的這麽直白,讓我來說:免疫係統為基因載體護過航後,在很多情況下就開治做壞事了,從腦裏的多發性硬化症到腿的類風濕性關節炎, 可以折磨得你痛不欲生。 ADE多見於Flavivirus, 風頭正鍵的華大病毒學家Michael Diamond起家的病毒種類,像在泰國流行的登革熱或南美流行的Zika。登革熱病毒重複感染可以加重病情,如果出現體液滲出症那可是致命性的。但是ADE也存在於冠狀病毒,薩斯和中東冠狀病毒都有ADE的報道。 在日本的三大生物醫學重鎮(京都大學、東京大學和大阪大學)中,大阪大學的免疫學是最好的。因為發現IL-6的Tadamitsu Kishimoto在那裏坐鎮幾十年,當然他的輝煌成就是與他在美國的訓練密切相關的。從這點上看,我們應該選擇相信這篇來自大阪的文章, 文章的前二位作者應該都是中國人。 我隻有時間講這日本大阪工作的大概,大家可以結合看我後麵以前文章,去理解這裏所說的ADE。寫這種文章我是兩頭不討好的,上篇文章居然有位不太懂免疫學的專業人士,錯誤地指出我說的通俗易懂的內容。 這項工作最為驚奇的發現是,造成新冠病毒感染力增強的抗體,不是來自我們通常認為的抗新冠病毒的非中和性抗原,而是直接抗中和性的S蛋白的抗體。我們知道S蛋白作為中和抗原的原因是因為它兼具與ACE2受體結合和隨後的攻膜功能,所以我們打的輝瑞和Moderna疫苗都是針對S蛋白設計的。 大阪大學通過篩選新冠病人抗其實S蛋白區域的抗體發現,病人中存在的抗S蛋白N末端的多種抗體,能夠十分明顯地增加S蛋白與ACE2的結合力度,可以增加高達三倍。常見的D614G突變型已經增加了受體結合力,而抗N端抗體能再增加這種結合力三倍左右。他們還證明,這種增加的受體結合強度可以直接導致病毒的感染性增加。他們做了競爭實驗和抗體結合位點的結構定位,所有資料都相互支持結論。 更加令人擔憂的是,他們在所測定的所有病人樣品中都發現了這種具有ADE的抗體,從圖譜上數他們至少做了10位新冠病人。這些擁有ADE的抗體隻抗N末端區域,抗其他區域的抗體沒有增加病毒感染的功能。這也可以理解因為N端在外麵,受體結合區域(RBD)就在它的下遊,它們直接協調涉及與ACE2受體的結合效力。 日本研究組還在48位非感染者中發現了3位擁有這種功能的抗體,說明有些人預先就存在抗這個S蛋白N末端的抗體。這個也好理解,因為冠狀病毒早就存在於自然界,人們在不知不覺中就感染過,交叉反應使我們擁有抗體。但是這些人如果感染了新冠病毒,病情就會特別重,雪上加霜。 這些還要補充說說,新冠就是淘汰弱基因型的自然選擇壓力,很殘酷但是我們隻有麵對。現在是免疫缺陷症患者的壓力時刻,像最近發現的幹擾素缺陷的病人如果感染新冠,那就十分不幸了,幹擾素及其受體係統是抗病毒之王。我們能活還是死,有時就是天命注定的,後麵有科學的支持,但是我們隻知道那麽一點點,絕大部分我們都不明白,看你人類還是否繼續無限度地破壞自然的生態環境。 我們以前都認為ADE是滅活疫苗的擔心,這個研究如果被證實,打輝瑞和Moderna疫苗的人也有可能不能幸免增強的病毒感染,如果大家的體內因為疫苗誘導了這類抗體的話。現在各種途經研發的疫苗,幾乎都是希望誘導產生對S蛋白的抗體,所以這個發現是對所有疫苗的挑戰。 輝瑞疫苗是抗整段S蛋白的,Moderna可能編碼的S蛋白短些,但是它們應該都應該產生抗N末端的抗體。解決這個問題的辦法會迫使BioNTech或Moderna重新設計他們的mRNA順序,以避免編碼出的S蛋白含有N末端,這樣刺激產生的抗體就不會有ADE。但是這也有個擔心,如果新疫苗不識別N末端很有可能會影響疫苗的有效性,因為N端可能協助RBD與受體結合的。但是對於滅活疫苗就遠沒有這麽方便了,找到N末端缺陷的病毒並且大量培養它們做新代的疫苗難上加難,所以滅活疫苗麵對ADE十分頭痛。 但是日本結果不能解釋輝瑞疫苗和Moderna疫苗的亮麗臨床三期結果,為什麽在疫苗組反複感染時都沒有出現加重的現象?現在應該這樣說,再漂亮的科學都有落實到臨床試驗的結果,能夠具有保護力就是王道。 同濟在美國做執業藥師的校友補充到:“現在緊急上市以後的四期臨床數據將有助回答這個問題,這是為什麽現在的疫苗隻達到緊急許可。這個後期數據(普通疫苗需一般是兩年的數據)的缺失就是風險所在,不過從現在疫情和三期數據來看,打疫苗依然是正確選擇。” 可從我以前的文章了解關於ADE的背景知識, 不能不佩服新冠的ADE又被華大前病理主任猜中了: “聖路易斯華大的前病理係主任Skip Virgin在Nature上發表長篇評述,談及新冠病毒可能存在的抗體依賴的病毒增強效應(ADE)。雖然現在還沒有確切地證明ADE在新冠中存在,但是這種可能性已經讓我們警覺,所以這篇評述必將成為熱讀的文章。我們總是失去這樣優秀的人才,傳說Skip是在競爭哈佛或華大醫學院院長失敗後才萌生的去意,現在Vir做SVP,工資是CEO的2-3倍。 弄懂ADE的機理必須知道抗體的兩個大致的結構,一個是Fc, 另一個為Fab。Fc通過與細胞膜上的Fc受體結合將抗體吸附在細胞膜上,Fab端則通常是抗體與病毒抗原結合的地方。也就是說抗體通過Fc受體的內吞功能將與Fab端結合的病毒帶入細胞內,這是ADE現在的機理解釋。中和抗體去執行消滅病毒,或阻止病毒與細胞受體粘附結合。具有ADE功能的抗體通常是親和力低的非中和抗體,有些具有交叉反應性。當然,這個也不能絕對化,低親和力的中和抗體也可能產生ADE。 但是抗體除了中和病原外,它們還可以通過與Fc受體結合和活化補體以產生免疫效應功能。這些功能也參與抗病毒免疫,比方說補體產生趨化作用和增強吞噬功能等,有時這些效應也導致自身免疫性疾病。這是阿肯森經常說的一句話,在人類認識淋巴細胞之前,免疫學家除了研究抗體就是玩的補體,補體能夠輔助抗體的產生。 人類關於Fc受體的大部分知識來自一個地方,洛克菲勒大學的Jeffrey Ravetch 實驗室,早應該授予他諾貝爾獎了,今天才知道他本科也是耶魯的。他人很難相處,但是為十分聰明的猶太人。Fc受體當然是起免疫活化功能的多,現在認為擁有四種活化性的Fc受體,但是Ravetch的傑出貢獻包括發現了抑製的Fc受體(FcRIIB),所以這套複雜的受體係統也存在內在的平衡。另一個新穎的Fc受體稱為初生Fc受體,它能夠使抗體或其他循環蛋白的半衰期延長,也通過樹突狀細胞的內吞免疫複合物的功能使抗體循環應用,備受製藥公司的親睞。 現在發現在呼吸道合胞病毒,麻疹和登革熱都出現了ADE,抗體增強的病毒感染。ADE可以通過三種途經獲得:前期的自然感染,打了疫苗以及為了治療輸入的抗體。這三種途徑都有一個共同點,那就是機體裏存在針對病毒的抗體。這些抗體所形成的免疫複合物正好能活化補體的經典途經,所以遭遇ADE的病人的組織裏通常會伴隨補體C4d的沉澱。對於新冠病毒的ADE可能性小的支持證據是,ACE2和Fc受體一般不會同時在細胞上表達,但是現在更多受體發現後就難說了”。 |