製造祖傳不孕不育症,第一顆“基因炸彈”炸響
?最近,《自然·生物(Nature Biotechnology)》刊載了一篇論文。英國倫敦帝國理工大學(Imperial College London)的研究人員宣布,通過基因編輯技術,在實驗蚊子中傳播“絕育”基因,最快隻用7代蚊子,就完全消滅了一個蚊子種群。

消滅蚊子就是實驗預期的目的。岡比亞按蚊傳播瘧疾,所以研究人員想發明一種快速滅蚊方法。但是,僅僅通過自發繁衍,就能讓人為編輯的特定基因迅速擴散,最終消滅整個種群,這種技術展示的技術潛力可不僅僅是防治瘧疾那麽簡單。
一 誰家祖上是太監?
經過郭德綱和網民的演繹,“祖傳不孕不育症”已經成了著名的互聯網段子。這個笑話背後隱含了一個幾乎無可辯駁的進化論原理——如果某種基因會影響生殖能力,它必然會在自然界迅速滅絕。所以,在自然生物種群中插入先天不孕個體,對整個種群影響不大。
但英國科學家恰恰要把這條看似“不可能”的路走通,通過擴散一種不孕基因,讓族群中的母蚊子不能生育,達到種群滅絕的目的。
實驗用到了兩項當前最火的基因編輯技術:“基因剪切”和“基因驅動”。簡單來說,“基因剪切”可以剪掉不要的基因,還可以粘貼上需要的基因;而“基因驅動”能夠大大增加某個基因被繼承的概率,讓指定基因在有性生殖中傳給下一代的可能性遠大於1/2。
兩者結合,就能讓某個特定的基因,以最快速度擴散。
二 非正常繁衍
實驗分為兩部分:第一步,剪掉蚊子胚胎中的一段基因,看看胚胎長大後是否不孕。第二步,設法讓所有蚊子都帶上這種基因。
在第一步實驗中,科學家通過“基因剪切”得到了4種蚊子:半殘公蚊子、半殘母蚊子、全殘公蚊子和全殘母蚊子。
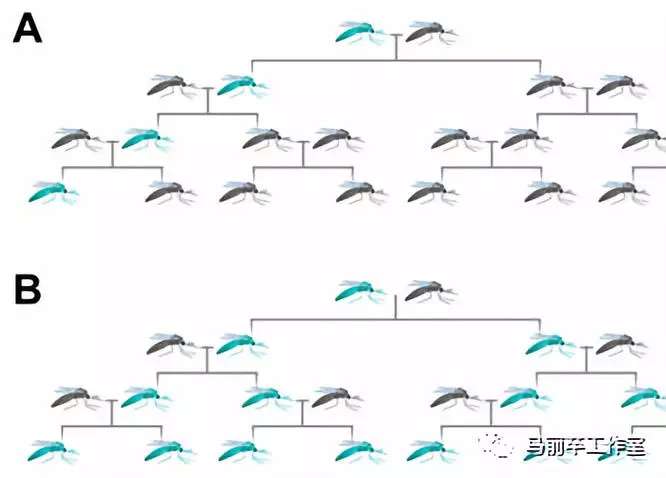
他們和正常蚊子的對比圖如下:

6種蚊子當中,隻有全殘的母蚊子不能生育,所以目標是讓全殘母蚊子占據足夠高的比例。
為了實現這個設想,科學家設計了第二步實驗:
他們模擬自然投放環境,把1200隻蚊子分成兩組,安置到兩個完全一樣的實驗箱中。每個箱子裏有300隻正常母蚊子、150隻正常公蚊子和150隻半殘公蚊子。這裏的半殘公蚊子比第一步的更甚一籌。科學家運用“基因驅動”技術,讓他們更容易生出殘疾子女。殘疾的子女繼續生出殘疾的孫子輩、殘疾的曾孫……直到生不出來。
三 氣死孟德爾
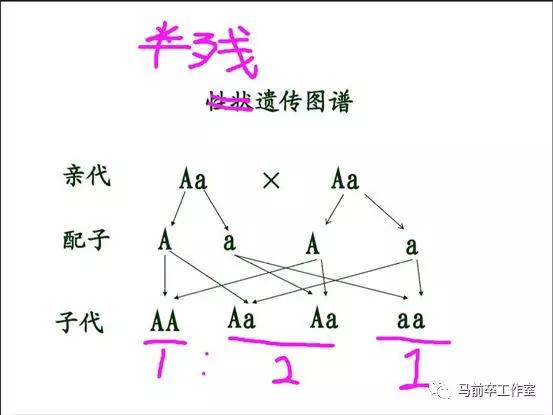
複習下高中生物教給我們的孟德爾原理,正常情況下基因傳遞概率是這樣的:
正常X正常 ——> 正常
半殘X正常 ——> 正常:半殘=1:1
半殘X半殘 ——> 正常:半殘:全殘=1:2:1 正常蚊子有1/4。
全殘公X正常母 ——> 半殘
任何公X全殘母 ——> 絕後
根據這個規律,用不了幾代,正常蚊子就會淘汰半殘種群
但這些半殘蚊子都經過基因驅動技術的改造,實際發生的情況是:
正常X正常 ——> 正常
半殘X正常 ——> 半殘:正常=9:1
半殘X半殘 ——> 正常:半殘:全殘(正常比例未知,但肯定不是四分之一)
全殘公X正常母 ——> 半殘
任何公X全殘母 ——> 絕後
總之,隻要父母有一方是半殘蚊子,那後代有9成是半殘蚊子。尤其是半殘媽媽,幾乎肯定不會生出半殘子女。孟德爾看不懂的遺傳公式出現了。
四 基因武器
這意味著半殘蚊子固然容易絕後,但在絕後之前,總是在下一代中傳播了更高比例的絕育基因。所以每一代蚊子都會生出更高比例的殘疾蚊子,最終......
不難看出,致殘基因擴散速度將輕鬆超過半殘蚊子的死亡速度。而半殘蚊子越多,全殘母蚊子產生的概率就越大。
看下圖:
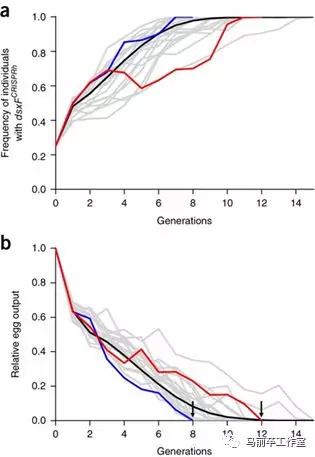
如圖所示,紅箱子裏的第8代蚊子已經無法再產卵,藍箱子繁衍到第12代也不再產卵,全都在擬合的預測範圍內。人類第一套基因武器通過了測試。
五 殺傷有限
不過,別急著扔掉你的蚊帳。因為這套武器還很不成熟。
“基因驅動”和“基因剪切”分別誕生於2002年和2012年。手持利器,科學家立刻就考慮如何花樣“虐”蚊。
主要思路如下:
1)給蚊子注入抗傳染病基因,讓每隻蚊子都成為“衛生”蚊子。
2)利用基因驅動,使蚊子隻生某一性別的子孫,讓蚊子種群性比失衡
3)設法讓蚊子帶上不孕不育基因,斷子絕孫。
4)剪掉蚊子的其他基因,比如降低蚊子的視力和飛行能力,讓他們無力傳播疾病。
以上每一項研究,都信誓旦旦“有望滅絕蚊子”,但這個在地球上生活了1億年的昆蟲,生命力異常頑強。這些方法要麽需要反複投放,太麻煩;要麽目前技術難以實現;要麽是蚊子很快產生基因突變。即便某種手段對一種蚊子有效,換一個亞種,基因編輯又失效了。
比如本文的主角,倫敦帝國理工大學,也反複意識到自己的技術局限性:
“因為以字母M和S區分的岡比亞按蚊亞種在外表上幾乎一模一樣,卻存在大量深層基因差異,這些差異使它們的發育、進食和繁殖習性都不相同,對其中一種蚊子有效的防治手段,未必對另一種蚊子有效。”
六 未來會怎樣?
以往談到基因武器的時候,人類總是想針對特定基因開發出一種病菌,感染包含指定基因的生物。至於病菌傳播,還得靠其他工具拋入目標種群,和傳統武器區別不大。但這次通過基因驅動技術,英國科學家成功地把生物的正常繁衍變成了傳播工具,等於在種群內部投下了一顆“遺傳炸彈”,殺傷半徑隨著蚊子的繁衍而不斷擴大,最終消滅整個種群。
夏天被蚊子咬的時候,每個人都期盼能一揮手消滅所有蚊子。但當人類真的掌握了這種能力,卻很少有人敢隨手扔出基因炸彈——因為我們不知道爆炸的後果。不說在人類種群中釋放基因炸彈會怎樣,就算我們能把殺傷範圍控製在蚊子一種生物,恐怕也不知道有多少食物鏈上的其他生物會被波及,會有多少地區的生態平衡發生不可逆的改變。所以,即便武器測試成熟,遺傳炸彈也必須在無比嚴謹的考察下才能釋放。
但基因編輯技術的擴散,卻是不可逆的趨勢。因為人類並不是一種為現代生活“定做”的生物。現代人希望“逆天而行”,希望活五百歲,又要生活精致,還要保持健康……這本身就不符合生老病死的自然規律,為基因編輯技術提供了強大的需求。所以,除了對付蚊子,很多國家已經在老鼠、狗、豬、羊……乃至人類身上開展試驗。
韓國基礎科學研究所基因工程中心的科學家們,剛剛使用CRISPR-Cas9對活鼠視網膜支撐組織進行了“基因手術”。2015年,中國科學家通過去肌肉生長抑製素基因基因創造了兩個超級肌肉小獵犬。

?2016 年,四川大學的醫療團隊開展了人體首例基因編輯(基於 CRISPR)的臨床試驗。
還有商人開始兜售自行注射的基因編輯器:
最近由Do-It-Yourself (DIY)生物黑客發起的眾籌活動引起了眾多關注。生物黑客初創公司Odin在其網站上銷售DIY Bacterial CRISPR試劑盒,零售價為159美元。2017年10月,Odin的首席執行官Josiah Zayner在於舊金山舉行的合成生物學會議上為自己注入了CRISPR改造肌肉生長的基因。
https://baijiahao.baidu.com/s?id=1593190189780591649&wfr=spider&for=pc

?2015年的前三個月裏,基因剪切技術技術相關的成果如潮水一般的湧來,單從NCBI上的數據就可以看出,發表的論文已經達到了上萬個,從成果上來說,不但在衰老研究,癌症研究方法取得了重要成果,而且技術上也突破了一個個難題。
七 未來會怎樣?
過去幾百年,任何先進技術,都會首先應用於軍隊,基因炸彈也一樣——對基因編輯技術投資最大的國家機構,正是大名鼎鼎的美國DARPA,中文全稱“美國國防高級研究計劃局”。
2017年,DARPA宣布了總額6500萬美元的Safety Gene計劃,支持美國加州大學河濱分校、哈佛醫學院、麻省理工等在內的7家國內研究機構進行基因編輯技術研究。這還隻是在美國國內,在英國帝國理工的論文末尾,同樣鳴謝了DARRA的資助。
DARPA宣稱“這筆投資中的絕大多數將會用於設計更安全的係統,以及可以抵抗或逆基因驅動產品的工具,防止有一天這種技術有意或無意地被釋放到野外。”
在基因編輯技術得以安全應用之前,我們還有其他防禦措施嗎?
目前看,還得靠傳統的門禁和保安。美國加州大學河濱分校的昆蟲學家 Omar Akbari 每天上下班都需要穿過六扇鐵門和一間隔離室。倫敦帝國理工大學的基因編輯實驗室同樣設有六道門,並需要兩級安全門禁權限才能進出。
這六道鐵門,在未來很長一段時間裏,將是遺傳炸彈與自然界之間的全部隔離,也是基因武器和恐怖分子之間的全部防線。


